Fenoloj
Fenolo | |||||
 | |||||
Plata kemia strukturo de Fenolo | |||||
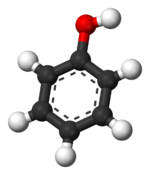 | |||||
Tridimensia kemia strukturo de Fenolo | |||||
 | |||||
Kristaloj de Fenolo. | |||||
Alternativa(j) nomo(j) | |||||
| |||||
| Kemia formulo | C6H5OH | ||||
| CAS-numero-kodo | 108-95-2 | ||||
| ChemSpider kodo | 971 | ||||
| PubChem-kodo | 996 | ||||
| Merck Index | 15,7354 | ||||
Fizikaj proprecoj | |||||
| Aspekto | trabiveblaj kristaloj | ||||
| Molmaso | 94,113 g·mol-1 | ||||
| Denseco | 1,071g cm−3 | ||||
| Fandpunkto | 43 °C | ||||
| Bolpunkto | 181,7 °C | ||||
| Refrakta indico | n76120{displaystyle n_{761}^{20}} 1,5425 | ||||
| Ekflama temperaturo | 83 °C | ||||
| Memsparka temperaturo | 79 °C | ||||
| Solvebleco | Akvo:67 g/L | ||||
| Mortiga dozo (LD50) | 80 mg/kg (buŝe) | ||||
Sekurecaj Indikoj | |||||
| Riskoj | R20/21/22 R23/24/25 R34 R48 R68 | ||||
| Sekureco | S24/25 S26 S28 S36/37/39 S45 | ||||
Pridanĝeraj indikoj | |||||
Danĝero
| |||||
| GHS Damaĝo Piktogramo |
| ||||
| GHS Signalvorto | Damaĝa | ||||
| GHS Deklaroj pri damaĝoj | H301, H311, H314, H318, H331, H341, H373, H411 | ||||
| GHS Deklaroj pri antaŭgardoj | P201, P202, P260, P261, P264, P270, P271, P273, P280, P281, P301+310, P301+330+331, P302+352, P303+361+353, P304+340, P305+351+338, P308+313, P310, P311, P312, P314, P321, P330, P361, P363, P391, P403+233, P405, P501[1] | ||||
Escepte kiam indikitaj, datumoj estas prezentataj laŭ iliaj normaj kondiĉoj pri temperaturo kaj premo (25 °C kaj 100 kPa) | |||||

Kemia strukturo de salikata acido, aktiva parto de aspirino.

Strukturo de cinamata acido.
La fenoloj estas membroj de tiu organika kombinaĵ-familio, en kiuj unu hidroksilgrupo (OH) aliĝas al karbono, kiu estas membro de benzolringo aŭ alia aromata ringo konsistanta el karbonatomoj. La nomo fenolo ne estas nur grupnomo de diversaj kombinaĵoj. Oni nomas ankaŭ fenolo la plej simplan membron de la familio, la monohidroksi-benzolon (C6H5OH) (ankaŭ nomata karbolatacido).
La fenoloj similas al la alkoholoj, sed en fenoloj la oksigena atomo estas forte ligita kun la aromata ringo, kaj la ligo inter la hidrogena kaj oksigena atomoj estas do malpli forta, ol en alkoholoj. Pro tio la fenoloj solviĝas en la akvo pli bone kaj la bolpunkto estas pli alta. Ili havas acidan pH-n.
La fenoloj estas - en ĉambra temperaturo - aŭ senkoloraj likvaĵoj aŭ blankaj solidaĵoj. Multaj fenoloj havas pikan, spican odoron. La monohidroksi-benzolo havas agrablan, dolĉetan odoron, sed ĝi estas tre venena kaj kaŭtera.
Produkto |
Oni produktas la t.n. naturan monohidroksi-benzolon el ligna gudro aŭ karba distilado, sed la kombinaĵo estas ankaŭ gajnebla el nafto aŭ el plantoj. La pluaj fenoloj troviĝas en volatila oleo de plantaj grajnoj kaj folioj. Oni pli frue produktis la sintezitajn fenolojn el karbogudro, sed nun oni produktas ilin per benzolo.
Reago |
La acidaj fenoloj reagas kun la fortaj bazoj kaj formas diversajn alkal-metalsalojn – fenoksidojn, fenolatojn aŭ fenatojn. La plej grava reago de la monohidroksi-benzolo estas la kondensado kun formaldehido (aperas ankaŭ akvo). Oni produktas laŭ tiu reago al sintezajn polimerojn, fenol-formaldehid-rezinojn kaj el tiuj plastajn artiklojn.
Oni uzas la fenolojn ankaŭ kiel purigaĵoj, desinfektaĵoj.
Kombinaĵoj |
- Kalia fenoksido
- Kanabinoido
- Natria orto-fenila fenolo
- Psilocibino
- Tirozino
| ||||
↑ Pubchem







